Infodemia (del inglés infodemic [1]) es el término que la Organización Mundial de la Salud acuñó para alertar de la propagación masiva de desinformación en el contexto de la pandemia provocada por el virus SARS-CoV-2. En este sentido, los profesionales de la salud jugamos un rol destacado como fuente de información, veraz, actualizada y basada en la evidencia. Con esta finalidad se ofrece esta pertinente visión general de la información disponible sobre los Equipos de Protección Respiratoria (EPR) más utilizados durante la crisis sanitaria [2].
Hace unos días se publicaba la Orden SND/422/2020 [3] en la que se dispone, con carácter general, el uso obligatorio de mascarillas en personas de 6 años en adelante en la vía pública, en espacios al aire libre y en cualquier espacio cerrado de uso público o que se encuentre abierto al público, siempre que no sea posible mantener una distancia de seguridad interpersonal de al menos 2 metros, siendo recomendable su uso para la población infantil de entre 3 y 5 años.
Luchamos comunitariamente en la contención de un virus aerotransportado por medio de gotitas procedentes de las secreciones de las membranas mucosas (las llamadas “gotitas de Flügge”) que todos expelimos al hablar, toser, estornudar e incluso respirar, y para minimizar el impacto que su enfermedad (denominada COVID-19) provoca. Entre las medidas establecidas para contener su propagación se encuentra la utilización de mascarillas [4] [5] [6] de manera racional [7], responsable [8] y optimizada [9], huyendo de la falsa sensación se seguridad que podrían otorgarnos. En esta lucha resulta fundamental seguir cumpliendo con el resto de medidas preventivas y de contención recomendadas por los organismos e instituciones oficiales, sin olvidar que las medidas de protección colectiva son prioritarias sobre las medidas de protección individual.
Por diferentes aspectos tales como su utilización para otros fines específicos, la incomodidad de su uso durante largos periodos de tiempo o el mayor coste, no serán objeto de mención las medias máscaras con filtro, las máscaras, los cascos, los capuces ni los sistemas de equipos filtrantes o aislantes. Por tanto, en el contexto que nos ocupa, nos ceñiremos a la tarea de describir distintos aspectos en la utilización de mascarillas (también llamadas “medias máscaras” o “barbijos”), insistiendo en que no representan la única medida de protección y prevención de contagio.

Conviene aclarar que el marcado CE (Conformidad Europea) [10] es un marcado obligatorio para muchos productos que se comercializan en la Unión Europea (UE). Demuestra que el fabricante ha evaluado el producto y se considera que éste cumple los requisitos de seguridad, sanidad y protección del medio ambiente exigidos por la UE. El marcado CE es igualmente obligatorio para los productos fabricados en cualquier lugar del mundo que vayan a comercializarse en la UE.
TIPOS DE MASCARILLAS
Las mascarillas son adaptadores faciales que cubren nariz, boca y barbilla, debiendo garantizar el máximo ajuste con la cara del usuario, para lo que cuentan con un arnés de cabeza, de tipo banda, cinta o cordón ajustable rodeando la cabeza o sujetándose en las orejas, para una firme y cómoda utilización. Se componen básicamente de material filtrante y de un adaptador facial. Además, pueden contar con un clip, pinza o puente nasal para mejorar la adaptabilidad alrededor del contorno de la nariz.
En caso de ser población vulnerable [11] (personas mayores de 60 años, diagnosticadas de hipertensión arterial, diabetes, enfermedades cardiovasculares, enfermedades pulmonares crónicas, cáncer, inmunodeprimidos y durante el embarazo por el principio de precaución), se recomienda usar el tipo de mascarilla según indicación médica, y como norma general, no está indicado el uso de mascarillas en niños menores de 3 años.
Según su diseño, distinguimos entre horizontales (o de pico-pato), verticales, cónicas (con forma de copa) y moldeadas.
En base a sus especificaciones técnicas, podemos distinguir entre:
- MASCARILLA HIGIÉNICA, no médica, de barrera o comunitaria.
- MASCARILLA QUIRÚRGICA o médica.
- MASCARILLA AUTOFILTRANTE, EPI, media máscara filtrante o de alta eficacia.
- MASCARILLA DUAL (quirúrgica + autofiltrante).
MASCARILLA HIGIÉNICA.

Este producto no tiene la consideración de producto sanitario ni de equipo de protección individual, sino que se considera una medida higiénica
complementaria, como puede ser el lavado de manos, la etiqueta respiratoria, el distanciamiento físico entre personas o evitar tocarselas mucosas.
Las mascarillas higiénicas son piezas faciales desechables (unsolo uso) no herméticas que suelen estar compuestas por una o varias
capas de material textil no tejido o combinación de materiales
(algodón, viscosa, popelina,…), en cuyo caso la capa filtrante debería ir situada en el medio y, si la combinación es bicapa, la capa filtrante debería situarse como capa exterior.
Están indicadas en:
- Población general sana (sin contacto con positivos por COVID-19) o sin síntomas que no sean susceptibles de utilizar mascarillas quirúrgicas o autofiltrantes (esta indicación resulta ser particularmente relevante en situaciones epidémicas/pandémicas, cuando el número de personas asintomáticas pero infecciosas se puede suponer que es alto en la comunidad).
- En caso de utilizar mascarillas, los niños sanos a partir de 3 años, deberían utilizarlas acorde a cada rango de edad en función de la talla: pequeña (3-5 años), mediana (6-9 años) o grande (10-12 años).
- Niños con síntomas o asintomáticos positivos por COVID-19 podrían utilizar mascarillas higiénicas con especificación UNE para evitar ser transmisores del virus.No están indicadas en trabajadores sanitarios.
Las mascarillas higiénicas pueden ser de los siguientes tipos:
1.- Mascarillas higiénicas que cumplen las especificaciones UNE 0064 o 0065:
- No Reutilizables (NR) para adultos (sus métodos de ensayo se rigen por la Norma UNE 0064-1) y para niños de 3 a 12 años (Norma UNE 0064-2). Deben ser desechadas después del uso recomendado por el fabricante. Por razones de comodidad e higiene, se suele recomendar no usar la mascarilla durante más de 4 horas. En caso de que se humedezca o se deteriore por el uso, se recomienda sustituirla por otra.
- Reutilizables (R). Sus métodos de ensayo se rigen por la Norma UNE 0065. El fabricante indicará el número máximo de lavados a partir de los cuales no se garantiza su eficacia.
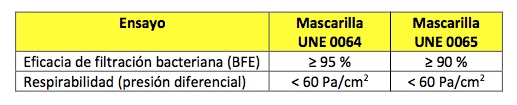
2.- Mascarillas higiénicas con otras especificaciones: se someten a ensayos y no llegan a cumplir el estándar de calidad UNE o simplemente han hecho ensayos en base a otras normas. Pueden indicar en su etiquetado que se han sometido a estas pruebas y mostrar los resultados obtenidos.
3.- Mascarillas higiénicas sin especificaciones o “caseras” [12]: no se han sometido a ensayos ni verificaciones. La evidencia que respalda el uso de mascarillas caseras como medida de prevención es limitada [13], pero sí existen estudios que apuntan a que su uso como último recurso puede ser mejor que no usar nada [14].
Según la Orden SND/354/2020 [15], los datos mínimos exigibles en el etiquetado de todo tipo de mascarillas higiénicas comercializadas son:
– Datos de la empresa fabricante: nombre, razón social y domicilio.
– Denominación usual del producto.
– Contenido del envase: número de unidades si el envase contiene varias mascarillas.
– Composición.
– Periodo recomendado de uso.
– Características esenciales del producto, incluyendo la talla en caso de ser pertinente, ysi es reutilizable o de un solo uso. Si se trata de una reutilizable debe indicarse unnúmero de lavados máximo, así como un método de lavado e higienización.
– Advertencias, entre ellas: “Este producto no es un equipo de protección individual ni unproducto sanitario”.
– Lote de fabricación cuando el proceso de elaboración se realice en series identificables.
– Instrucciones de uso sobre colocación, uso y mantenimiento, manipulación yeliminación.
– Lugar de procedencia u origen, en el caso de que su omisión pudiera inducir a error alconsumidor.
– Si cumple las especificaciones técnicas UNE 0064-1:2020, UNE 0064-2:2020 o UNE0065:2020 o cualquier norma equivalente.
– Los datos testados relativos a la BFE y de respirabilidad en caso de que se haya realizadotest, incluyendo el número de ensayo y el laboratorio empleado.
– El precio final completo, incluidos los impuestos, desglosando, en su caso, el importe de los incrementos o descuentos que sean de aplicación a la oferta y los gastos adicionalesque se repercutan al consumidor o usuario.
Limpieza y desinfección de mascarillas higiénicas reutilizables:
En ausencia de recomendaciones por parte del fabricante, el Ministerio de Sanidad recomienda tres posibles métodos [16]:
- Realizar un ciclo completo de lavado en la lavadora (humedecer, lavar, enjuagar) con el detergente habitual y agua a temperatura entre 60°-90°.
- Sumergir las mascarillas en una dilución de lejía 1:50 (20 mL de lejía en 980 mL de agua)con agua tibia durante 30 minutos. Después lavar con agua y jabón y aclarar bien para eliminar cualquier resto de lejía y dejar secar.
- Desinfectar las mascarillas con un producto virucida autorizado para superficies, de acuerdo a las instrucciones del fabricante, poniendo especial atención al uso diluido o no del producto y a los tiempos de contacto necesario para la actividad desinfectante. Una vez desinfectadas las mascarillas, se lavarán con abundante agua y jabón para eliminar cualquier resto químico y se dejarán secar.
MASCARILLA QUIRÚRGICA

Es una pieza facial desechable (de un solo uso) no hermética (sin requerimiento de ensayo de ajuste) que tiene la consideración de Producto Sanitario (PS) de la clase I. Generalmente dispone de una capa que actúa como filtro colocada, unida o moldeada, entre capas de tela. Suelen componerse de tres capas: la exterior, que actúa como repelente de fluidos (normalmente coloreada), la intermedia, como barrera contra gérmenes, y la interior, como absorbente de la humedad.El nivel de eficacia que ofrecen depende de factores como la eficacia de filtración, la calidad del material y la adaptabilidad a la cara del usuario. Las mascarillas quirúrgicas pueden tener formas y construcciones diferentes, así como características adicionales tales como un escudo facial para proteger a quien la lleva contra salpicaduras de fluidos potencialmente contaminados (no implica protección frente a la inhalación de un aerosol líquido), o función antiniebla. Estas mascarillas filtran el aire espirado, proporcionando una barrera para minimizar la transmisión de agentes infecciosos procedentes de la persona que la lleva puesta. Los métodos de ensayo se rigen por la Norma UNE-EN 14683.
Están indicadas en:
– Población general en casos de epidemia/pandemia para reducir el riesgo depropagación de infecciones (en caso de no suponer un recurso crítico).
– Niños y adultos sintomáticos o asintomáticos positivos por COVID-19.
– Personas que han estado en contacto estrecho con positivos por COVID-19 en losúltimos 14 días.
– Las mascarillas quirúrgicas de tipo II y IIR están indicadas para profesionales sanitariosque trabajen en un quirófano o en otro entorno médico con requisitos similares.
Al ser consideradas productos sanitarios, se rigen por lo dispuesto en el Real Decreto 1591/2009 [17] (el Reglamento 2017/745 [18] será aplicable a partir del 26 de mayo de 2021). El tiempo de uso depende de lo indicado por el fabricante, aunque por cuestiones de comodidad e higiene, se suele recomendar no usar la mascarilla durante más de 4 horas. En caso de que se humedezca o deteriore por el uso, se recomienda sustituirla por otra.
Las mascarillas quirúrgicas se deberían comercializar en su envase primario original (caja dispensadora o equivalente) pero, en base a la Orden SND/354/2020, las oficinas de farmacia podrán vender mascarillas quirúrgicas individualmente sin empaquetar, siempre y cuando se garanticen unas condiciones de higiene adecuadas que salvaguarden la calidad del producto. Dicha medida durará hasta que lo determine el Ministerio de Sanidad. En base a la Resolución de 22 de abril de 2020 [19], se fijó el precio de venta al público unitario en 0,96 euros.
En base a los diferentes ensayos a los que se someten, podemos clasificarlas en tipo I, tipo II y tipo IIR:
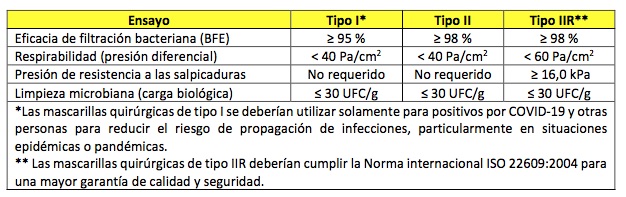
En el envase primario original debe aparecer:
- Denominación o nombre comercial del producto.
- Nombre del fabricante (o representante autorizado) y dirección.
- Número de autorización de la AEMPS.
- Presencia del marcado CE.
- Norma europea EN 14683.
- Tipo de mascarilla (tipo I, II o IIR).
- Lote de fabricación.
- Fecha límite de utilización.
- Cantidad de productos contenidos.
Marcado CE:
El fabricante, a efectos de la colocación del marcado CE, deberá realizar, de acuerdo con la clase de producto sanitario de que se trate, uno o varios procedimientos de evaluación de la conformidad.
Las mascarillas quirúrgicas, al ser PS de la clase I (no estériles y sin función de medición), el procedimiento de evaluación de la conformidad será la “declaración CE de conformidad”, donde no interviene ningún Organismo Notificado [20] (ON), por lo que la evaluación se realiza bajo la exclusiva responsabilidad del fabricante. El marcado CE no llevará asociado ningún número, salvo que la mascarilla se ofrezca como estéril (en este caso deberá indicar el número del ON que ha evaluado las condiciones de esterilidad del producto).
La Orden SND/326/2020 [21] establece que, hasta la finalización del estado de alarma y en interés de la protección de la salud, la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS), como ON 0318, podrá autorizar de forma expresa la puesta en el mercado y la puesta en servicio de mascarillas quirúrgicas para las cuales no se hayan satisfecho los procedimientos de evaluación relativos a la colocación del marcado CE.
MASCARILLA AUTOFILTRANTE
Es una pieza facial hermética (ensayo de ajuste requerido) que tiene la consideración de Equipo de Protección Individual (EPI) de la categoría III (según el riesgo a proteger para el que estén diseñados, los EPI pueden ser de Categoría I, II o III) según el Real Decreto 1407/1992 [22], por lo que deben cumplir con el Reglamento (UE) 2016/425 [23]. Las mascarillas de protección individual cubren nariz, boca y mentón, filtran la inspiración y protegen frente a la inhalación de bioaerosoles (suspensión de partículas sólidas o líquidas de origen biológico en el aire). Sus métodos de ensayo se rigen por la Norma UNE-EN 149.
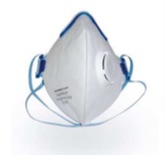
Estas mascarillas pueden disponer de una o varias válvulas de exhalación, que permiten que el aire exhalado salga directamente sin pasar por el material filtrante y cuya finalidad es facilitar la respiración, ayudando a disipar el calor, la humedad y el CO2 que se genera en el interior de la mascarilla.
Están indicadas en personas que cuiden o estén en contacto estrecho y prolongado con pacientes sintomáticos o asintomáticos positivos por COVID-19. Las mascarillas con válvula de exhalación no están indicadas en pacientes con infección activa.
La denominación de estas mascarillas autofiltrantes sigue la siguiente nomenclatura: FF + P + NR/R + D, donde FF es la notación de “media máscara filtrante”, P denota el tipo de filtración (frente a partículas y aerosoles) y su clase (1, 2 o 3), NR (para un solo turno de trabajo o no reutilizable) o R (para más de un turno o reutilizable). D denota haber superado un ensayo de obstrucción con dolomita y es una notación opcional para las NR y obligatoria para las R.
La Norma EN 149 establece una serie de requisitos y ensayos (de fuga, de inflamabilidad, de obstrucción, etc.) y clasifica en tres posibles niveles a las mascarillas filtrantes de protección contra partículas, en función de su rendimiento y de su fuga hacia el interior en:
1.- Mascarillas FFP1: tienen una eficacia de filtración mínima del 78%, y un porcentaje de fuga hacia el interior máximo del 22%. No se recomiendan para uso médico, y se suelen utilizar frente a partículas de material inerte.
2.- Mascarillas FFP2: en este caso la filtración mínima es del 92%, con un porcentaje de fuga hacia el interior máximo del 8%. Estas mascarillas se usan frente a aerosoles de baja o moderada toxicidad. Están indicadas para quienes cuiden (se incluye la toma de muestra con torunda nasofaríngea [24]) o estén en contacto estrecho con personas sintomáticas o positivos por COVID- 19, principalmente personal sanitario.
3.- Mascarillas FFP3: la filtración mínima de este tipo de mascarillas se eleva al 98%, mientras que el porcentaje de fuga hacia el interior es solo del 2%. Estas son las recomendadas ante aerosoles de alta toxicidad. Según las recomendaciones de Sanidad, están indicadas en el personal sanitario que atienda en situaciones en las que se generen aerosoles que favorecen el contagio (casos de intubación traqueal, lavado broncoalveolar o ventilación manual).
Todo EPI comercializado debe disponer de:
- Marcado CE.
- Documento de conformidad del EPI.
- Documentación con instrucciones e información relevante como lote, número de serie, número tipo.
Esta información debe ser visible en la propia mascarilla autofiltrante (obligatorio para todos los EPI de clase III) y constará de las letras del marcado CE seguidas de cuatro dígitos que identifican al Organismo Notificado. Por tanto, además del marcado CE seguido de los cuatro dígitos, estas mascarillas deben estar identificadas individualmente con:
- Nombre, marca registrada u otros medios de identificación del fabricante o suministrador.
- El tipo de mascarilla: FFP1, FFP2 o FFP3 + NR/R + D (cuando corresponda).
- La referencia a la norma armonizada aplicada: UNE-EN 149.
Limpieza y desinfección de las mascarillas autofiltrantes reutilizables:
Como norma general, solo se debe limpiar y desinfectar el ajuste con la cara, nunca elmaterial filtrante. En este sentido, un estudio evaluó la persistencia de del SARS-CoV-2 en las superficies y mostró que el virus se encuentra viable durante un máximo de 72 horas [25]. Una posible estrategia de reutilización (planteada por el CDC americano en caso de escasez) podría ser la de asignar 5 mascarillas a cada profesional sanitario para ser utilizadas de forma rotatoria en cada turno de trabajo (lo que garantizaría que desde el anterior uso hubiera transcurrido un lapso de tiempo superior a 72 horas), siempre y cuando se almacenen de forma segura y adecuada.La limpieza, desinfección y secado de las mascarillas reutilizables debe ser acorde con las recomendaciones del fabricante, teniendo en cuenta el método a aplicar y el número máximo de lavados para los que el fabricante garantiza las prestaciones de la mascarilla.Se debe evitar el contacto entre una mascarilla sucia (a lavar) y la ropa limpia. Procure lavar las mascarillas tan pronto como sea posible tras su uso. La persona a cargo del lavado debe protegerse para manejar las mascarillas sucias. Además, no se deben utilizar productos que puedan degradar o dañar los materiales y que disminuyan su capacidad protectora [26].Según los datos y evidencias que existen hasta el momento [27], las recomendaciones son las siguientes:
- Desinfección a altas temperaturas: no se deben secar o higienizar con un horno microondas. Las mascarillas EPI se ensayan después de llevar a cabo un tratamiento térmico prolongado, por lo que estas mascarillas (sin válvulas de exhalación) mantienen su eficacia de filtración después de llevar a cabo una desinfección a 70°C durante 30 minutos. Los EPR que en el proceso de certificación no hayan sido ensayados bajo condiciones de acondicionamiento a altas temperaturas, deberían estudiarse previamente a la recomendación de este método de desinfección.
- Desinfección con alcohol pulverizado: puede inactivar la retención electrostática de las fibras y originar una disminución de la eficacia de filtración por debajo del 95%.
- Desinfección con uso de vapor a 134°C: diversos estudios muestran que puede dar lugar a una disminución de la eficacia de filtración, así como producir la deformación de la mascarilla afectando al ajuste con la cara del usuario.
- Desinfección con vapor de peróxido de hidrógeno: la desinfección una y dos veces con un ciclo corto no ha mostrado deformación de la mascarilla ni alteración del ajuste con la cara; con un tercer ciclo de desinfección se observó deformación.
- Lavado con agua o soluciones jabonosas: puede causar deformación de la mascarilla y afectar al ajuste con la cara.
- Desinfección con microondas: no se tienen datos concluyentes sobre la influencia de este método. Sería necesario hacer pruebas para comprobar si la eficacia de filtración del material no se ve afectada.
- Desinfección por radiación UV germicida: el virus es sensible a rayos UV y, en principio a dosis bajas, no afectaría la eficacia de filtración. Estudios realizados con dosis más altas, a pesar de su mayor eficacia, muestran un aumento de la penetración y deterioro del material.
En todos los casos, se recomienda que los procesos de desinfección se lleven a cabo sobre mascarillas individualmente. Después de cada ciclo de lavado, se debe realizar una inspección visual (con guantes o manos lavadas). Si se detecta algún daño en la mascarilla (menor ajuste, deformación, desgaste, etc.), se debe desechar la mascarilla.
Es recomendable también que la reutilización de las mascarillas sea siempre por parte de la misma persona.
– Secado: se recomienda que la mascarilla se seque completamente dentro de las 2 horas posteriores al lavado. Tanto durante el secado, como en el almacenamiento posterior de la mascarilla, se deben evitar los ambientes en los que la mascarilla se pueda volver a contaminar. No se debe utilizar la mascarilla si está sucia o húmeda.
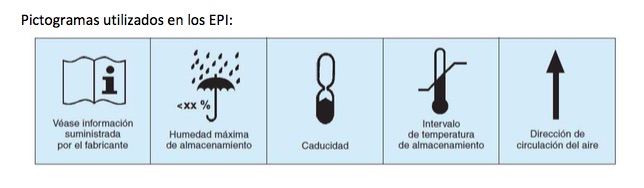
Marcado CE:
Las mascarillas autofiltrantes, como EPI que son, deben llevar marcado CE conforme al Reglamento 2016/425. Esto implica que el fabricante debe elaborar una Declaración UE de conformidad y además, el EPI debe llevar la información que se indica en el Reglamento: datos del fabricante, identificación del producto (número de lote…), instrucciones e información, etc.
En el caso de mascarillas EPI, previamente a la puesta del marcado CE, interviene un ON durante el procedimiento de evaluación de la conformidad. Dicho ON realizará un examen UE de tipo y emitirá un Certificado de examen UE de tipo. Además de esto, el fabricante también debe tener un control de la producción, cuyos detalles varían en función de la categoría del EPI.
La Resolución de 23 de abril de 2020 [28], considerando la situación de escasez de EPI con el marcado CE reglamentario, autoriza temporalmente a que las mascarillas no lleven “marcado CE”, ampliando el listado de normas consideradas como equivalentes hasta que se complete la evaluación de las conformidades necesarias para poner el marcado CE a dichos productos o hasta el 30 de septiembre de 2020 (lo que antes ocurra).
MASCARILLA DUAL
Es una pieza facial hermética desechable que proporciona protección frente a bioaerosoles a la persona portadora y a la vez reduce la transmisión de
agentes infecciosos de esta misma persona al exterior. Tiene la
consideración de PS y de EPI, por lo que debe cumplir las disposiciones legislativas de ambos (incluido el marcado CE). Estarían indicadas en el cuidado de pacientes en aislamiento respiratorio (y en todas aquellas situaciones en las que sea necesario “proteger y protegerse”).
EQUIVALENCIAS INTERNACIONALES
Existen distintas normas técnicas a nivel internacional sobre mascarillas autofiltrantes y distintos procesos de certificación o aprobación. Cada norma exige unos requisitos técnicos o especificaciones a cumplir.
Las especificaciones técnicas [29], distintas de las normalizadas, que se considera que ofrecen un nivel adecuado de protección conforme a los requisitos esenciales de salud y seguridad establecidos en el Reglamento (UE) 2016/425, al objeto de obtener el marcado CE son las siguientes:
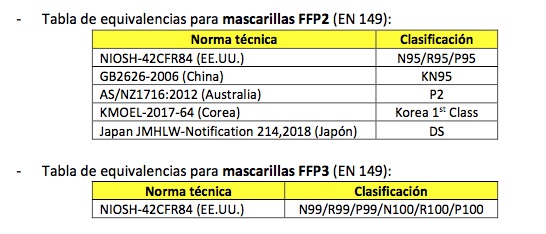
Las denominadas “mascarillas faciales” N95 están reguladas por la U.S. Food and Drug Administration (FDA) cuando se destinan a un propósito médico (prevenir enfermedades). Los materiales utilizados en la fabricación de las mascarillas quirúrgicas deben cumplir las especificaciones de la Norma ASTM F2100 Standard Specification for Performance of Materials Used in Medical Face Masks de la American Society of Testing and Materials (ASTM). Existen numerosos recursos en línea [30] que determinan requisitos, ensayos, eficacia y métodos de desinfección para este tipo de mascarillas.
Mención aparte merecen las especificaciones para las mascarillas KN95. Y es que, sus normas de fabricación y su nomenclatura, son ligeramente diferentes al resto del mundo. Simplificando, en China se distingue entre lo que es una mascarilla facial para uso médico y las que no tienen ese uso.Debido a la crisis sanitaria, el Gobierno chino dio la orden de que todas las mascarillas fueran verificadas en tres aspectos: eficacia de penetración, resistencia a la respiración y marcado. En consecuencia, todas las mascarillas que hay en el mercado chino deberían tener informes de ensayo con estos tres resultados, realizados por el National Quality supervision and testing center for personal protective equipment. Cada provincia china tiene al menos uno de estos laboratorios que están acreditados.En la actualidad, la acreditación otorgada por el CNAS (China National Accreditation Service for Conformity Assessment [31]) a los laboratorios para la prueba de mascarillas incluye los estándares chinos y los estándares EN:
– Norma GB/T 32610: establece estándares chinos recomendados a nivel nacional para mascarillas higiénicas desechables de uso diario frente a partículas ≤ 2,5 micras. Suelen ser utilizadas por la población de China para protegerse de la contaminación ambiental y no están indicadas para actividades médicas.
– Norma YY/T 0969-2013: establece estándares chinos recomendados en la industria farmacéutica para mascarillas médicas de protección general en ambiente clínico.
– Norma YY 0469-2011: establece estándares chinos obligatorios en la industria farmacéutica para lo que podrían ser mascarillas quirúrgicas de tipo IIR. Tendrían una posible equivalencia con la Norma EN 14683:2019+AC:2019.
– Norma GB 19083-2010: establece estándares chinos obligatorios a nivel nacional para las mascarillas de protección para uso médico.
– Norma GB 2626-2006: establece estándares chinos obligatorios a nivel nacional para mascarillas autofiltrantes KN/KP 90/95/100. Tendría una posible equivalencia con la Norma UNE-EN 149. Esta Norma, en principio, la aplica el propio fabricante en un proceso de autocertificación bajo su propia responsabilidad y la vigilancia del mercado es la que actúa en su caso.
VERIFICACIONES
La Recomendación (UE) 2020/403 [32] reconoce que determinados EPI y PS (se incluyen tanto las mascarillas quirúrgicas como las autofiltrantes) son esenciales para los trabajadores sanitarios, los servicios de primera intervención y el resto del personal que participa en los esfuerzos por contener el virus y evitar su propagación. Insta a que los Estados miembros adopten todas las medidas adecuadas para garantizar que los EPI o los PS que no lleven el marcado CE, y que puedan introducirse en el mercado de la Unión, solo se pongan a disposición de los trabajadores sanitarios.
Para poder aceptar un producto sin el marcado CE, con limitación temporal a la crisis y disponible solo para el personal sanitario, el agente económico que corresponda deberá presentar la documentación que avale el cumplimiento con la especificación que alegue, así como información sobre el proceso de certificación/aprobación establecido en el mercado que corresponda. Por tanto, los supuestos establecidos para la aceptación de EPI sin marcado CE son:
1.- Compra o adquisición pública de EPI sin marcado CE conforme al apartado 8 de laRecomendación (UE) 2020/403: los EPI solo podrán ser suministrados al personal sanitario durante la crisis en curso. La verificación del producto se realizará por la autoridad contratante o aceptante durante el proceso de compra o aceptación de la donación.
2.- Autorización temporal: se autoriza la comercialización de EPI sin marcado CE que cumplan especificaciones técnicas distintas de las normas armonizadas establecidas en el Anexo de laResolución de 23 de abril de 2020.La validez se suspenderá si se constata que el producto no cumple las especificaciones técnicas a través de la vigilancia del mercado o de la evaluación de conformidad por un ON. Las autorizaciones temporales se concederán por las autoridades de vigilancia de mercado, incluido el ámbito aduanero. Dicha autoridad evaluará que el producto cumple con las especificaciones del Anexo de la Resolución. Para realizar la evaluación, las autoridades podrán solicitar a un ON español para elReglamento (UE) 2016/425 que evalúe la documentación aportada y cualquier otro aspecto que considere.
Verificaciones para mascarillas EPI [33]:
Podemos seguir algunas indicaciones generales para poder verificar la idoneidad de la documentación que acompaña a las mascarillas EPI que pudiera avalar un nivel adecuado de protección de la salud y seguridad para los usuarios.
Es importante poder verificar la trazabilidad del certificado/informe de cumplimiento con una especificación técnica con el producto concreto.
Certificados UE de tipo (de acuerdo con el Reglamento 2016/425):
Deben estar emitidos por un ON de los listados en la base de datos NANDO [35]. Es importante recordar que un organismo puede estar notificado para el Reglamento de EPI pero no para el campo concreto del equipo que se certifica (p.ej. los equipos que proporcionan protección al sistema respiratorio) o no en el módulo adecuado, en cuyo caso el certificado no sería válido.
Las mascarillas de protección biológica son EPI de categoría III: en la declaración de conformidad debe indicarse el ON que hace el examen UE de tipo (módulo B) y el que realiza el control de la producción (módulos C2 o D). La declaración de conformidad debe acompañar al equipo o permitir acceder a ella a través de un enlace incluido en el folleto informativo.
Existen numerosos “certificados de conformidad” emitidos por entidades que no son ON o que aun siendo ON no lo son para la normativa de EPI. Estos certificados no son válidos a estos efectos. Normalmente estos certificados no indican los 4 dígitos que identifican al ON.
Ante la creciente sospecha y confirmación de certificados falsos o no válidos emitidos para mascarillas EPI [34], debemos comprobar la veracidad de dichos documentos. Hasta la fecha se han identificado y comunicado entre las autoridades de los Estados miembros que los certificados emitidos por las siguientes entidades no son válidos: CELAB, ICR Polska, ISET, ECM y NPS.
Información mínima que debe contener el certificado de examen UE de tipo:
- Nombre y número de identificación del ON.
- Nombre y dirección del fabricante.
- Identificación del EPI objeto del certificado.
- Declaración de que el tipo del EPI cumple los requisitos esenciales de salud y seguridad aplicables.
- En el caso de que se hayan aplicado total o parcialmente normas armonizadas, las referencias de dichas normas o partes de las mismas.
- En el caso de que se hayan aplicado otras especificaciones técnicas, sus referencias.
- Si procede, el nivel o los niveles de rendimiento o la clase de protección del EPI.
- La fecha de expedición, la fecha de expiración.
- Respecto a los EPI de categoría III, una declaración de que el certificado se utilizará únicamente junto con uno de los procedimientos de evaluación de la conformidad de la producción (módulo C2 o D).
USO ADECUADO
Para una correcta utilización de la mascarilla deberemos acudir siempre a las instrucciones o a la ficha técnica del producto. Como norma general,
siempre deberemos seguir las siguientes recomendaciones:
1.- Antes de ponernos una mascarilla debemos desinfectarnos correctamente las manos con agua tibia y jabón o con gel desinfectante que contenga alcohol en un porcentaje superior al 60% durante 40-60 segundos. Debemos procurar tocar solo el arnés de cabeza (las gomas o cintas) de la mascarilla.
2.- Comprobaremos que la mascarilla está colocada correctamente, verificando el sellado y la ausencia de molestias respiratorias. Es necesario llevarla puesta de tal manera que cubra la nariz y la boca del usuario, recomendándose colocar la mascarilla sobre la piel desnuda (es poco probable que se consiga un buen ajuste si el vello facial se encuentra sobre la zona de sellado facial).
3.- Durante el periodo de uso de la mascarilla solo se puede utilizar una o varias veces si se retira de acuerdo con las instrucciones, se almacena temporalmente o se cuelga para ofrecer el menor contacto posible, y se vuelve a colocar siguiendo las instrucciones. Dado que las mascarillas utilizadas se consideran altamente contaminadas, es esencial que el cuerpo de la mascarilla no se toque con las manos. Nunca ha de dejarse una mascarilla en posición de espera en la frente o debajo de la barbilla durante o después de su uso. Cuando exista una necesidad adicional de protección, el usuario se debería poner una mascarilla nueva.
4.- Como norma general, los equipos de protección respiratoria deben retirarse en último lugar, tras la retirada de otros componentes como guantes, batas, etc. Debemos quitarnos la mascarilla procurando tocar únicamente el arnés de cabeza, sin tocar la parte frontal.
5.- Una vez retirada, procederemos a su correcta eliminación.
6.- Por último, nos desinfectaremos las manos.
CORRECTA ELIMINACIÓN
La mascarilla utilizada se debería desechar cuando ya no se necesite o haya superado el número máximo de lavados (en el caso de reutilizables) en un contenedor provisto de una bolsa de plástico (preferiblemente con tapa y apertura no manual) o en los contenedores para residuos biológicos.
La Orden SND/271/2020 [35] establece medidas sobre la gestión de residuos en domicilios, hospitales, centros de salud, laboratorios, ambulancias y establecimientos similares.
CONCLUSIONES
Las indicaciones establecidas para el uso generalizado de mascarillas deben seguir el principio de precaución, puesto que su uso pretende conseguir un adecuado nivel de protección en función de la situación epidemiológica en las que nos encontremos. El sentido común, basado en la evidencia científica, debe guiarnos en el uso racional y responsable de estos recursos que han llegar a tener la consideración de críticos por su escasez en el mercado.
En el ámbito sanitario, no debemos confundir los equipos destinados a evitar la contaminación del material estéril, con los destinados a la protección del trabajador, usándose aquéllos como protecciones personales frente al riesgo biológico, cuando en la mayoría de situaciones no solo no son eficaces, sino que provocan la sensación de falsa protección frente al riesgo (un ejemplo típico en este sentido es la utilización de mascarillas quirúrgicas para la protección frente a la inhalación de un bioaerosol infeccioso).
FUENTES DE INFORMACIÓN
[1] Zarocostas, John (29-02-2020). How to fight an infodemic [en línea]. The Lancet. Vol 395. [Consulta: 17-05-2020]. Disponible en: https://www.thelancet.com/action/showPdf?pii=S0140- 6736%2820%2930461-X
[2] Real Decreto 463/2020, de 14 de marzo, por el que se declara el estado de alarma para la gestión de la situación de crisis sanitaria ocasionada por el COVID-19. Disponible en: https://www.boe.es/buscar/pdf/2020/BOE-A-2020-3692-consolidado.pdf
[3] Orden SND/422/2020, de 19 de mayo, por la que se regulan las condiciones para el uso obligatorio de mascarilla durante la situación de crisis sanitaria ocasionada por el COVID-19. Disponible en: https://www.boe.es/boe/dias/2020/05/20/pdfs/BOE-A-2020-5142.pdf
[4] Interim guidance (06-04-2020). Advice on the use of masks in the context of COVID-19. World Health Organization [en línea]. [Consulta: 17-05-2020]. Disponible en: file:///C:/Users/Usuario/Downloads/WHO-2019-nCov-IPC_Masks-2020.3-eng%20(2).pdf
[5] ECDC Technical report (08-04-2020). Using face mask in the community. European Center for Disease prevention and Control [en línea]. [Consulta: 17-05-2020]. Disponible en: https://www.ecdc.europa.eu/sites/default/files/documents/COVID-19-use-face-masks-community.pdf
[6] Centro de coordinación de alertas y emergencias sanitarias (20-04-2020). Recomendaciones sobre el uso de mascarillas en la comunidad en el contexto de COVID-19. Ministerio de Sanidad [en línea]. [Consulta: 17-05-2020]. Disponible en: https://www.mscbs.gob.es/profesionales/saludPublica/ccayes/alertasActual/nCov-China/documentos/Recomendaciones_uso_mascarillas_ambito_comunitario.pdf
[7] Interim guidance (06-04-2020). Rational use of personal protective equipment for coronavirus disease (COVID-19). World Health Organization [en línea]. [Consulta: 17-05-2020]. Disponible en: https://apps.who.int/iris/bitstream/handle/10665/331695/WHO-2019-nCov-IPC_PPE_use-2020.3- eng.pdf?sequence=9&isAllowed=y
[8] ¿Qué debes tener en cuenta al comprar una mascarilla? Ministerio de Consumo [en línea]. [Consulta: 17-05-2020]. Disponible en: https://www.lamoncloa.gob.es/serviciosdeprensa/notasprensa/consumo/Documents/2020/030520%20 GU%C3%8DA%20COMPRA%20MASCARILLAS.pdf
[9] National Center for Immunization and Respiratory Diseases (NCIRD), Division of Viral Diseases (18-05- 2020). Strategies to Optimize the Supply of PPE and Equipment. CDC Center for Disease Control and Prevention [en línea]. [Consulta: 20-05-2020]. Disponible en: https://www.cdc.gov/coronavirus/2019- ncov/hcp/ppe-strategy/index.html
[10] Marcado CE (15-04-2020). Web oficial de la Unión Europea [en línea]. [Consulta: 19-05-2020]. Disponible en: https://europa.eu/youreurope/business/product-requirements/labels-markings/ce- marking/index_es.htm?pk_campaign=YEB_Search2019- 20&pk_medium=banner9&pk_source=google_es&_pmclid=b_10715621_wp_3980839_k_3466735
[11] National Center for Immunization and Respiratory Diseases (NCIRD), Division of Viral Diseases (14- 05-2020). People who are at higher risk for severe illness. CDC Center for Disease Control and Prevention[en línea]. [Consulta: 20-05-2020]. Disponible en: https://www.cdc.gov/coronavirus/2019-ncov/need- extra-precautions/people-at-higher-risk.html
[12] Guías para la fabricación de mascarillas y ropa de protección. Ministerio de Industria, Comercio y Turismo [en línea]. [Consulta: 16-05-2020]. Disponible en: https://www.mincotur.gob.es/es-es/COVID- 19/Paginas/guias-para-fabricacion-de-mascarillas-y-ropa-de-proteccion.aspx
[13] Davies A [et al] (2013). Testing the efficacy of homemade masks: would they protect in an influenza pandemic? [en línea]. Disaster Med Public Health Prep. 2013;7(4):413-418. [Consulta: 17-05-2020]. Disponible en: https:// www.ncbi.nlm.nih.gov/pubmed/24229526
[14] National Center for Immunization and Respiratory Diseases (NCIRD), Division of Viral Diseases (03- 04-2020). Recommendation Regarding the Use of Cloth Face Coverings, Especially in Areas of Significant Community-Based Transmission. CDC Center for Disease Control and Prevention [en línea]. [Consulta: 20- 05-2020]. Disponible en: https://www.cdc.gov/coronavirus/2019-ncov/prevent-getting-sick/cloth-face- cover.html
[15] Orden SND/354/2020, de 19 de abril, por la que se establecen medidas excepcionales para garantizar el acceso de la población a los productos de uso recomendados como medidas higiénicas para la prevención de contagios por el COVID-19. Disponible en: https://www.boe.es/buscar/pdf/2020/BOE-A- 2020-4525-consolidado.pdf
[16] Limpieza y desinfección de mascarillas higiénicas reutilizables (15-04-2020) . Ministerio de Sanidad[en línea]. [Consulta: 17-05-2020]. Disponible en: https://www.mscbs.gob.es/profesionales/saludPublica/ccayes/alertasActual/nCov- China/documentos/Limpieza_y_Desinfeccion_mascarillas_higienicas_reutilizables_pdf.pdf
[17] Real Decreto 1591/2009, de 16 de octubre, por el que se regulan los productos sanitarios. Disponible en: https://www.boe.es/buscar/pdf/2009/BOE-A-2009-17606-consolidado.pdf
[18] Reglamento (UE) 2017/745 del Parlamento Europeo y del Consejo, de 5 de abril de 2017 sobre los productos sanitarios. Disponible en: https://eur-lex.europa.eu/legal- content/ES/TXT/PDF/?uri=CELEX:02017R0745-20200424&qid=1589931456728&from=ES
[19] Resolución de 22 de abril de 2020 2020, de la Dirección General de Cartera Común de Servicios del Sistema Nacional de Salud y Farmacia, por la que se publica el Acuerdo de la Comisión Interministerial de Precios de los Medicamentos de 21 de abril de 2020, por el que se establecen importes máximos de venta al público en aplicación de lo previsto en la Orden SND/354/2020, de 19 de abril, por la que se establecen medidas excepcionales para garantizar el acceso de la población a los productos de uso recomendados como medidas higiénicas para la prevención de contagios por el COVID-19. Disponible en: https://www.boe.es/buscar/pdf/2020/BOE-A-2020-4577-consolidado.pdf
[20] Base de datos NANDO sobre Organismos Notificados – Organismos Notificados en España. European Comission [en línea]. [Consulta: 19-05-2020]. Disponible en: https://ec.europa.eu/growth/tools- databases/nando/index.cfm?fuseaction=country.notifiedbody&cou_id=724
[21] Orden SND/326/2020, de 6 de abril, por la que se establecen medidas especiales para el otorgamiento de licencias previas de funcionamiento de instalaciones y para la puesta en funcionamiento de determinados productos sanitarios sin marcado CE con ocasión de la crisis sanitaria ocasionada por el COVID-19. Disponible en: https://www.boe.es/buscar/pdf/2020/BOE-A-2020-4322-consolidado.pdf
[22] Real Decreto 1407/1992, de 20 de noviembre, por el que se regulan las condiciones para la comercialización y libre circulación intracomunitaria de los equipos de protección individual. Disponible en: https://www.boe.es/buscar/pdf/1992/BOE-A-1992-28644-consolidado.pdf
[23] Reglamento (UE) 2016/425 del Parlamento Europeo y del Consejo, de 9 de marzo de 2016, relativo a los equipos de protección individual. Disponible en: https://eur-lex.europa.eu/legal- content/ES/TXT/PDF/?uri=CELEX:32016R0425&qid=1589631258919&from=ES
[24] Documento técnico (14-04-2020). Prevención y control de la infección en el manejo de pacientes con Covid-19. Ministerio de Sanidad [en línea]. [Consulta: 17-05-2020]. Disponible en: https://www.mscbs.gob.es/profesionales/saludPublica/ccayes/alertasActual/nCov- China/documentos/Documento_Control_Infeccion.pdf
[25] Van Doremalen, N [et al.]. Aerosol and Surface Stability of SARS-CoV-2 as Compared with SARS-CoV- 1. J New England Journal of Medicine, 2020. Disponible en: https://www.nejm.org/doi/full/10.1056/nejmc2004973
[26] Center for COVID innovation (01-05-2020). N95 Respirator Decontamination & Reuse [archivo de vídeo]. Disponible en: https://www.youtube.com/watch?v=55XHNwtElrw&feature=youtu.be
[27] National Center for Immunization and Respiratory Diseases (NCIRD), Division of Viral Diseases (30- 04-2020). Decontamination and reuse of filtering facepiece respirators. CDC Center for Disease Control and Prevention [en línea]. [Consulta: 20-05-2020]. Disponible en: https://www.cdc.gov/coronavirus/2019-ncov/hcp/ppe-strategy/decontamination-reuse- respirators.html
[28] Resolución de 23 de abril de 2020, de la Secretaría General de Industria y de la Pequeña y Mediana Empresa, referente a los equipos de protección individual en el contexto de la crisis sanitaria ocasionada por el COVID-19. Disponible en: https://www.boe.es/buscar/pdf/2020/BOE-A-2020-4651- consolidado.pdf
[29] Centro Nacional de Medios de Protección-INSST (18-03-2020). Comparativas de especificaciones técnicas aplicables a mascarillas autofiltrantes. Ministerio de Trabajo y Economía Social [en línea].[Consultado: 17-05-2020]. Disponible en: https://www.insst.es/documents/94886/693030/Comparativa+especificaciones+t%C3%A9cnicas+Masca rillas+%2820.03.20%29/a48446b9-cfd6-4456-9303-8d75d85a02dd
[30] N95Decon Research Document (24-04-2020). Technical Document for Public Use of Medical Masks and Cloth Masks. N95Decon [en línea]. [Consulta: 17-05-2020]. Disponible en: https://static1.squarespace.com/static/5e8126f89327941b9453eeef/t/5ea3b5859bc8f31a11f3deb5/15 87787141808/2020-04-24_N95DECON_Face_Mask_Technical_Report_v1_final.pdf
[31] China National Accreditation Service for Conformity Assessment [en línea]. [Consulta: 19-05-2020]. Disponible en: https://www.cnas.org.cn/english/
[32] Recomendación (UE) 2020/403 de la Comisión de 13 de marzo de 2020 relativa a la evaluación de la conformidad y los procedimientos de vigilancia del mercado en el contexto de la amenaza que representa el COVID-19. Disponible en: https://eur-lex.europa.eu/legal- content/ES/TXT/PDF/?uri=CELEX:32020H0403&from=ES
[33] Verificación de certificados/informes que acompañan a los EPI (03-05-2020). Ministerio de Trabajo y Economía Social [en línea]. [Consulta: 19-05-2020]. Disponible en: https://www.insst.es/documents/94886/712877/Verificaci%C3%B3n+de+certificados+o+informes+que+ acompa%C3%B1an+a+los+EPI/1f104b83-1456-4c14-b1c0-20517f3174d1
[34] COVID-19 (11-05-2020). Suspicious certificates for PPE. European Safety Federation [en línea]. [Consulta: 19-05-2020]. Disponible en: https://eu-esf.org/covid-19/4513-covid-19-suspicious-certificates- for-ppe
[35] Orden SND/271/2020, de 19 de marzo, por la que se establecen instrucciones sobre gestión de residuos en la situación de crisis sanitaria ocasionada por el COVID-19. Disponible en: https://www.boe.es/buscar/pdf/2020/BOE-A-2020-3973-consolidado.pdf
